À primeira vista, os seres vivos são muito diferentes entre si. Uma bactéria, um arquea, uma ameba, um fungo, uma árvore e um vertebrado aparentemente têm poucas características em comum.
De fato, acabamos de ressaltar suas diferenças. No entanto, eles têm uma base química comum. A primeira característica básica é a dependência de água.
Podemos afirmar, sem margem de erro, que a base da vida na Terra é a água, uma substância cuja molécula apresenta propriedades muito especiais. A vida depende ainda de outras moléculas, nas quais o carbono é um elemento de grande importância.
A água e suas propriedades emergentes
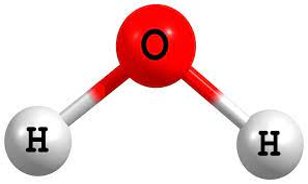
A água é representada pela conhecida fórmula molecular H2O, que significa que uma molécula dessa substância é formada por dois átomos de hidrogênio, ligados a um de oxigênio.
Existe uma desproporcional habilidade de atrair elétrons entre esses átomos, pois o átomo de oxigênio consegue “sugar” os elétrons dos dois átomos de hidrogênio da molécula.
Assim, uma parte da molécula de água está, de certa forma, rica em elétrons, enquanto outra parte está pobre, ou carente, deles, embora haja um equilíbrio na “contabilidade geral” de cargas elétricas na molécula.
A parte próxima ao núcleo do átomo de oxigênio tem um vestígio adicional de carga negativa, enquanto cada núcleo dos átomos de hidrogênio, parcialmente privado de seu respectivo elétron, passa a ter um vestígio adicional de carga positiva. Assim, a molécula de água fica polarizada.
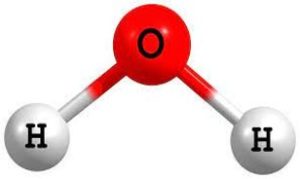
Como vimos, há duas partes positivas e uma negativa numa mesma molécula de água. Essa polaridade, em qualquer substância, já traria propriedades peculiares, mas na água e em outras substâncias em que o hidrogênio é atraído por elementos muito eletronegativos, como o oxigênio e o nitrogênio, aparece uma interação entre a parte positiva da molécula (os átomos de hidrogênio) e a parte negativa de moléculas vizinhas (os átomos de oxigênio ou nitrogênio), formando uma ligação de hidrogênio.
As ligações de hidrogênio também podem ser formadas entre moléculas de outras substâncias, além da água.
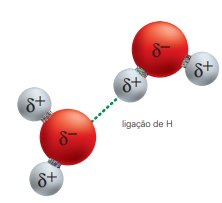
entre moléculas de água. Observe como a
parte negativa de uma molécula é atraída
pela parte positiva da molécula vizinha. No
estado líquido, as moléculas de água têm
grande agitação, e o átomo de oxigênio de
uma molécula pode manter uma ligação de
hidrogênio com outra molécula próxima.
Essas ligações, entretanto, não são muito fortes, o que permite a mobilidade das partículas típica do estado líquido, mas são suficientes para determinar um arranjo especial do conjunto de moléculas, devido à sua grande coesão – que explica, por exemplo, seu ponto de ebulição relativamente alto.
Se a água não apresentasse ligações de hidrogênio, ao nível do mar ela entraria em ebulição a uma temperatura muito inferior a 100 °C.
A manutenção da estrutura do material genético dos seres vivos depende de ligações como essas, formadas entre o átomo de hidrogênio de uma molécula e o átomo de oxigênio ou nitrogênio de outra molécula.
Antigamente utilizava-se a expressão “ponte de hidrogênio”. A representação gráfica dessa força intermolecular continua sendo uma linha com tracejado ou pontilhado, pois trata-se de uma ligação fraca, que pode ser rompida com pouca energia.
As ligações de hidrogênio formam-se em outros compostos polares, como o amônio, e mesmo em moléculas grandes, como os ácidos nucleicos e as proteínas.
Isso explica, por exemplo, por que a clara de ovo endurece com o calor: rompem-se ligações de hidrogênio e formam-se ligações mais estáveis na molécula de albumina.
Outra propriedade emergente é uma rigidez razoável da superfície de um pequeno volume de água líquida, a tensão superficial.
É a tensão superficial que permite a um inseto caminhar sobre uma poça de água sem molhar as pernas! A tensão superficial também explica por que se formam – e se mantêm – as gotas de água.
Quando observamos uma gota de óleo e uma gota de água, ambas sobre a mesma superfície, fica evidente a diferença de conformação das duas gotas, que pode ser explicada pela diferença da força de coesão molecular nas duas substâncias.
O peso dele não é suficiente para romper as ligações de hidrogênio entre as moléculas de água da superfície e fazê-lo afundar.
A água e os sais minerais
Outra extraordinária propriedade da água é a capacidade de atuar como solvente. Muitos átomos são carregados eletricamente, formando os íons. Íons com cargas positivas são denominados cátions, e íons com cargas negativas são chamados ânions.
O sal de cozinha é uma substância iônica composta por ânions de cloro (Cl–) e cátions de sódio (Na+). Na sua forma sólida, cada íon positivo está cercado de íons negativos e vice-versa.
Mas, se colocarmos um pouco desse sal na água, que tem moléculas com uma parte carregada positivamente e outra carregada negativamente, esses íons serão cercados por moléculas de água.
Os íons de cloro (Cl–, em lilás no esquema) serão envolvidos pela parte da molécula de água onde os átomos de hidrogênio (em alaranjado) sobressaem, e os íons de sódio (Na+, em verde no esquema) são cercados pela parte da molécula onde o átomo de oxigênio (em azul) sobressai.
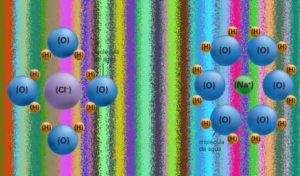
Essa característica da água faz com que ela seja um solvente extraordinário, capaz de transportar sais minerais na corrente sanguínea de diferentes animais e seres humanos, ou mesmo na seiva de plantas, além de atuar em inúmeras outras situações, como na erosão de rochas e na moldagem da paisagem. Um ser humano precisa diariamente de cerca de 500 mg de sódio e 750 mg de cloro.
Os sais minerais são importantes para a saúde humana. Veremos adiante os elementos químicos importantes para os organismos vivos, que podem se combinar em ligações iônicas, formando sais solúveis em água.
Sais de magnésio e potássio, por exemplo, são imprescindíveis para as plantas. Sais de cálcio e ferro, embora também importantes para as plantas, são necessários em quantidades relativamente maiores para os animais, em especial para os seres humanos.
Professor, alguns astrônomos afirmam que a amônia tem propriedades emergentes semelhantes às da água, em especial pelas ligações de hidrogênio que se estabelecem com os átomos de nitrogênio.
Como já se comprovou a presença de amônia em diversos planetas e satélites, acredita-se que a vida possa ter se organizado em bases diferentes em outros mundos.
Professor, embora os sais minerais (e as vitaminas) sejam estudados no volume 3 desta coleção, na parte referente à Nutrição Humana, uma rápida introdução é feita aqui. As necessidades diárias de sais minerais dos seres humanos se situam ao redor de: 2 000 mg (potássio), 1 000 mg (cálcio),
Professor, sais minerais e vitaminas não formam classes de substâncias, tal qual açúcares, proteínas e lipídios, que serão vistos adiante. No entanto,
como são compostos essenciais para a atividade celular, foram mencionados neste momento. O papel de algumas vitaminas será visto em mais detalhe adiante, ao focalizar o metabolismo energético, e em outro volume, ao focalizar a nutrição humana.
A água e as vitaminas
Os alimentos são fontes de sais minerais, participam de diversas reações químicas no organismo e são continuamente reaproveitados.
Além desses compostos iônicos, substâncias moleculares participam de reações químicas, acelerando-as sem serem consumidas.
São as chamadas vitaminas. Adiante veremos como o aproveitamento de energia dos alimentos depende da presença de vitaminas do complexo B, que são solúveis em água.
A vitamina C, muito comum em frutas cítricas, assim como as vitaminas do complexo B, também é solúvel em água.
Algumas vitaminas, no entanto, não são solúveis em água, como as vitaminas A, D e E, sendo por isso encontradas em alimentos gordurosos.
Resumo
- A água é uma substância básica para a manutenção da vida e tem propriedades emergentes que derivam de seu arranjo molecular. A coesão de suas moléculas é um exemplo de propriedade emergente.
- As ligações de hidrogênio formadas entre as moléculas da água conferem diversas propriedades emergentes a essa substância, muito importantes para os seres vivos.
- As ligações de hidrogênio entre moléculas estão na base de vários processos vitais, não apenas na água, envolvem hidrogênio, de um lado e, em geral, oxigênio ou nitrogênio de outro.
